1. 식약처 의료기기 신고 절차
신고대상 의료기기 품목 => 확인하기
1) 관련 법령
의료기기법 제6조(제조업), 제15조(수입업), 같은법 시행규칙 제7조
2) 절차 및 방법
접수 방법 : 구비서류를 갖추어 의료기기전자민원창구를 통해 인터넷 접수(http://emed.mfds.go.kr)하거나 의료기기정보기술지원센터에 직접 접수 ( 의료기기전자민원창구 → 회원가입 및 로그인 → 민원신청 → 전자민원안내 및 신청 → 의료기기 제조(수입)신고 민원신청)
3) 처리 기관
: 의료기기정보기술지원센터
4) 구비서류
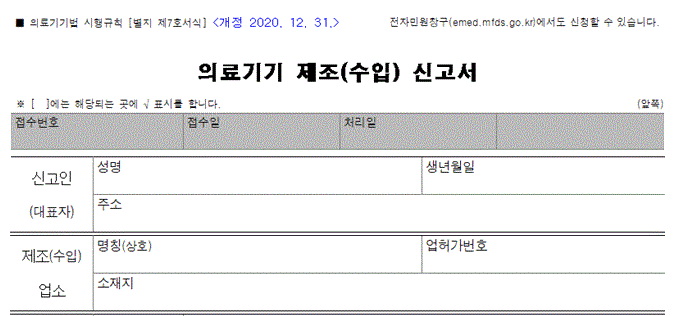
- 의료기기 제조(수입) 신고신청서 [별지 제7호서식] ※ 1등급 중 이미 허가를 받거나 신고한 품목과 구조, 원리, 성능, 사용목적 및 사용방법 등이 본질적으로 동등하지 않은 의료기기는 허가 신청해야 함.
- 전공정 위탁의 경우 수탁자 조건 증명서류(의료기기법시행규칙 별표2 제3호 가목에 따라 제조공정을 전부 위탁받을 수 있는자에 해당하는지 증명할 수 있는 서류
5) 작성 시 주의사항
- 품목류 신고대상의 경우 제조 신고 시 신고서의 “품목류”란에 표기를 하여야 한다. ※ 동일제품군에 해당하는 대표 제품 하나 이상을 대상으로 신청하여야 함.
- 사용목적 ‘의료기기 품목 및 품목별 등급에 관한 규정’ 「별표1」에 따라 기재하여야 한다
2. 식약처 의료기기 인증 절차
인증대상 의료기기 품목 => 확인하기
1) 관련 법령
의료기기법 제6조(제조업), 제15조(수입업), 같은법 시행규칙 제5 및 30조
2) 절차 및 방법
접수 방법 : 구비서류를 갖추어 의료기기전자민원창구를 통해 인터넷 접수(http://emed.mfds.go.kr) 하거나 식약처 종합민원실에 직접 접수 ( 의료기기전자민원창구 → 회원가입 및 로그인 → 민원신청 → 전자민원안내 및 신청 → 의료기기 제조(수입)인증·허가 민원신청)
3) 처리 기관 :
- 의료기기정보기술지원센터
4) 구비 서류
- 의료기기 제조(수입) 인증신청서 [별지 제5호서식]
- 기술문서 심사 결과 통지서 (발행일로부터 2년 이내)
- 일괄검토일 경우 : 기술문서 검토자료 및 허가신청 구비서류 전체
- GMP 신청서 사본 또는 당해 품목이나 동일품목군의 GMP 적합인증서 사본
- 전공정위탁일 경우 : 수탁자 조건 증명 서류(의료기기법시행규칙 별표2 제3호 가목에 따라 제조공정을 전부 위탁받을 수 있는 자에 해당하는지를 증명할 수 있는 서류

5) 참고사항
가). 동등공고제품
1) 식약처 공고 확인
2) 공고제품 비교
3) 시험검사 의뢰 ( 식약처 지정 의료기기 시험 검사기관)
4) 시험검사 성적서 발급
5) 제조업, 수입업 허가신청 (지방청) 및 기술문서 심사결과통지서 , 수탁자제조증명서류(제조업체의 해당자), GMP 적합인정서 신청 및 발급 (의료기기정보기술지원센터) => 신청 후 5일 이내 인증
■ 동등제품 판단기준(제23조 관련) => 확인하기
나). 동일제품
1) 동일제품 입증자료 제출 (의료기기 심사부)
2) 동일제품 확인 통보 (의료기기심사부)
3) 제조업, 수입업 허가신청 (지방청) 및 동일제품 통보 공문, GMP 적합인정서 신청 및 발급 (의료기기정보기술지원센터) => 신청 후 5일 이내 인증
다). 동등공고제품 및 동일제품이 아닌 그 외 의료기기 인증
1) 식약처 지정 기술문서심사기관에 기 허가 받은 제품과 비교 신청
2) 기술문서심사기관에서 심사결과통지서 발급
3) 기술문서 심사결과통지서 , 수탁자제조증명서류(제조업체의 해당자), GMP 적합인정서를 의료기관정보기술지워센터 인증 신청
4) 료기관정보기술지워센터에서 인증서 발급
3. 식약처 의료기기 허가 절차
1) 관련 법령, 절차 및 방법
위 인증 절차와 동일
2) 처리 기관
- 식품의약품안전처 식품의약품안전평가원 의료기기심사부
3) 처리 기간
- 안전성·유효성 심사필요 : 80일
- 기술문서 심사필요 : 65일
- 기술문서 등 심사불필요 : 10일
4) 구비 서류
- 의료기기 제조(수입) 허가신청서 [별지 제3호서식]
- 기술문서 심사 결과 통지서 (발행일로부터 2년 이내)
- 일괄검토일 경우 : 기술문서 검토자료 및 허가신청 구비서류 전체
- GMP 신청서 사본 또는 당해 품목이나 동일품목군의 GMP 적합인증서 사본
- 전공정위탁일 경우 : 수탁자 조건 증명 서류(의료기기법시행규칙 「별표2」 제3호 가목에 따라 제조공정을 전부 위탁받을 수 있는 자에 해당하는지를 증명할 수 있는 서류

4.. 식약처 지정 의료기기 시험 검사기관
=> 확인하기
5. GMP 심사 흐름도 (3,4등급)

'행정기관 인허가(등록신고)' 카테고리의 다른 글
| 폐기물 수집운반업 수집·운반차량 밀폐화 기준 및 적용사례 (0) | 2022.02.22 |
|---|---|
| 청주행정사 - 의료기기 비대면 체온계 수입업 허가 준비사항 (0) | 2021.12.29 |
| 야영장 허가를 통한 캠핑장 창업 허가 사전 검토 사항 (0) | 2021.12.15 |
| 임대사업자 등록 임대주택의 임대보증금 보증 가입 (0) | 2021.12.07 |
| 식품제조업, 접객업 등 식품관련 영업의 위생법상 허가 등록 신고 대상 업종 (0) | 2021.11.25 |




댓글